Pourquoi la batterie reste-t-elle le maillon faible du smartphone ?
Nous avons ici sur l’image trois iPhone, avec un écart de dix ans entre eux.
L’iPhone 12 est environ trois fois plus puissant que l’iPhone 6 en termes de performances, et l’iPhone 16 est environ deux fois plus puissant que l’iPhone 12.
Il y a donc une évolution très importante des performances, et c’est quelque chose de clair, car les performances progressent à un rythme rapide… sauf un élément qui, lui, ne progresse pas.
Si vous aviez un iPhone 6 et que je vous demandais combien de temps votre téléphone tient sans être rechargé, vous répondriez probablement entre une demi-journée et une journée.
La même chose s’applique à l’iPhone 12 : entre une demi-journée et une journée, et pour l’iPhone 16, c’est également la même chose, bien sûr selon votre usage.
Mais une chose reste évidente : tout évolue, sauf les batteries.
Pourquoi ?
Chaque année, on entend parler de téléphones plus rapides, de caméras plus performantes, d’écrans plus intelligents et d’intelligence artificielle toujours plus avancée.
Mais dès que l’on arrive à la batterie, il n’y a pas de progrès vraiment visible.
Le téléphone a toujours besoin d’être rechargé chaque jour, parfois même deux fois par jour, malgré tous ces progrès.
La question logique que se posent la plupart des utilisateurs est donc :
pourquoi n’avons-nous pas encore un téléphone qui fonctionne pendant plusieurs jours, voire une semaine, et qui se recharge en quelques minutes ?
La batterie d’un téléphone n’est pas un composant comme les autres, c’est un système chimique extrêmement délicat.
Le moindre changement peut légèrement améliorer les performances… ou tout détruire.
C’est précisément pour cette raison que l’évolution des batteries est lente par rapport aux autres composants du téléphone.
Un processeur peut être miniaturisé et amélioré par le logiciel, une caméra peut être optimisée par le calcul, mais la batterie est soumise à des lois physiques et chimiques strictes qui ne tolèrent pas l’erreur.
À l’intérieur de toute batterie lithium, on trouve quatre éléments fondamentaux :
- l’anode
- la cathode
- l’électrolyte
- et le séparateur
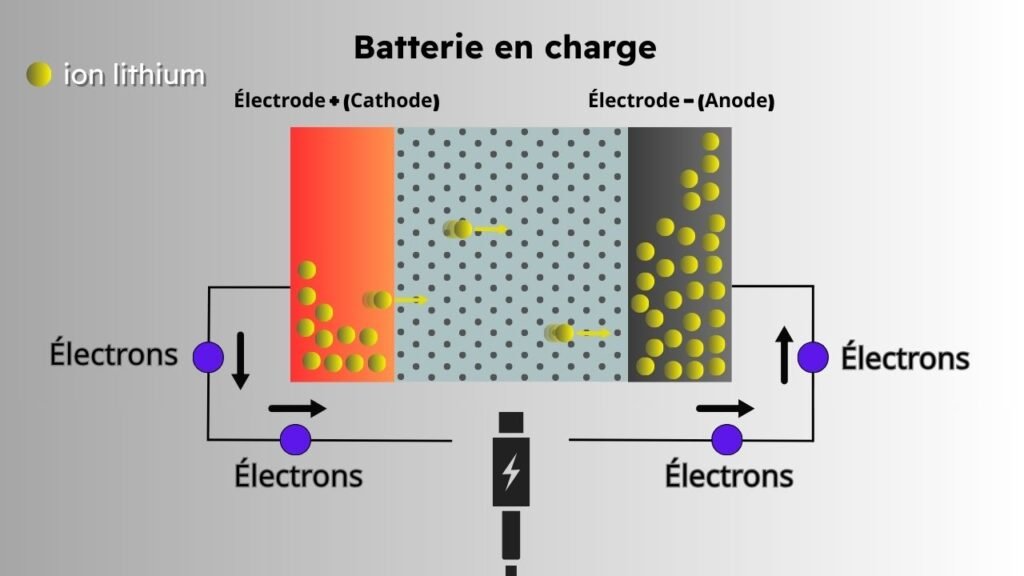
Sur le papier, le principe est très simple : lors de la charge, les ions lithium se déplacent de la cathode vers l’anode, et lors de l’utilisation, ils font le chemin inverse.
C’est ce mouvement qui permet de produire de l’électricité et de faire fonctionner votre téléphone.
Mais le problème est que ce mouvement doit être lent, stable et sûr, car le lithium est un élément extrêmement sensible.
L’anode est généralement fabriquée en graphite.
C’est l’endroit où les ions lithium « se logent » pendant la charge.
Mais ne peut-on pas simplement mettre plus de
lithium ?
C’est là que se trouve le premier véritable obstacle au progrès.
Le graphite a une capacité limitée pour accueillir le lithium.
L’anode finit par être saturée et, avec la charge rapide, de minuscules structures métalliques appelées dendrites peuvent se former.
Elles sont très dangereuses, car elles peuvent percer la batterie de l’intérieur et provoquer un court-circuit ou un incendie.
C’est pour cette raison que la charge rapide a toujours une limite, malgré ce que promettent les publicités.
La cathode est l’autre pôle de la batterie.
Elle est souvent composée d’un mélange de métaux comme le nickel, le cobalt et le manganèse.
Cette partie est responsable de la densité énergétique, c’est-à-dire de la quantité d’énergie que l’on peut stocker dans un volume réduit.
Le problème est qu’améliorer la cathode implique l’utilisation de matériaux plus sensibles, plus coûteux ou moins stables.
Par exemple, le cobalt est excellent pour les performances, mais il est cher et pose des problèmes éthiques, tandis que le nickel offre une densité énergétique plus élevée mais une stabilité thermique plus faible.
Chaque amélioration a donc un prix, soit en matière de sécurité, soit en durée de vie.
L’électrolyte est le « chemin » emprunté par les ions lithium entre l’anode et la cathode.
Il s’agit d’un liquide ou d’un gel inflammable, un point que beaucoup ignorent.
Accélérer la charge signifie accélérer le déplacement des ions dans ce liquide, ce qui génère de la chaleur.
Et chaleur plus liquide inflammable… je pense que vous comprenez la suite.
C’est pour cela que l’on entend souvent parler des batteries solides (solid-state), qui remplacent ce liquide par un matériau solide plus sûr.
Mais le problème est qu’elles restent difficiles à produire, très coûteuses et encore inadaptées à une production massive à grande échelle.
Quant au séparateur, c’est une couche extrêmement fine qui empêche l’anode et la cathode d’entrer en contact direct.
Cela peut sembler être un élément simple, mais c’est en réalité la dernière ligne de défense.
Le moindre dommage dû à la chaleur ou à la pression signifie la fin de la batterie.
Avec la charge rapide ou une utilisation intensive, ce séparateur s’use avec le temps, et c’est à ce moment-là que la batterie commence à se dégrader après un ou deux ans.
Une autre question se pose alors : pourquoi les entreprises ne repensent-elles pas
complètement ce système ?
La réponse honnête est que toute modification majeure de l’un de ces quatre éléments affecte directement les trois autres.
Une amélioration isolée peut déséquilibrer l’ensemble du système.
C’est pour cela que nous observons de petites améliorations progressives et très calculées, plutôt que de grands bonds en avant, contrairement aux processeurs ou aux caméras.
Pourtant, le téléphone moderne consomme plus d’énergie que jamais.
Les écrans à haute fréquence, les processeurs puissants, la photographie continue, l’intelligence artificielle fonctionnant en arrière-plan et les applications gourmandes en ressources… tout cela consomme énormément d’énergie.
Même une amélioration de 10 à 15 % de la batterie est rapidement annulée par l’intensité de l’usage actuel.
C’est pour cette raison que l’on a l’impression que les batteries « n’évoluent pas » : ce n’est pas qu’elles stagnent, mais que notre consommation augmente encore plus vite.
Aujourd’hui, les entreprises ne cherchent pas à créer une batterie révolutionnaire, mais à maintenir un équilibre global :
- une batterie sûre,
- qui dure plusieurs années,
- qui se recharge à une vitesse raisonnable
- et qui supporte un usage quotidien sans risques juridiques ou techniques.
En résumé, parvenir à un téléphone capable de fonctionner plusieurs jours et de se recharger en quelques minutes n’est pas impossible.
Mais cela nécessitera une véritable révolution dans la chimie des batteries.
Ce ne sera ni une mise à jour annuelle ni un progrès aussi rapide que certains l’imaginent.
Nous continuerons à voir des améliorations lentes et intelligentes, car jouer avec le lithium n’est pas anodin, la moindre erreur peut transformer un outil du quotidien en un réel danger dans votre poche.
Les batteries solides vont-elles résoudre le problème définitivement ?
Elles offrent un potentiel réel en matière de sécurité et de densité énergétique, mais leur production à grande échelle reste complexe et coûteuse. Elles ne remplaceront pas les batteries lithium-ion du jour au lendemain.
La charge rapide abîme-t-elle la batterie ?
Oui, partiellement. Elle accélère l’usure chimique à long terme en augmentant la température et le stress interne, même si les systèmes modernes intègrent des protections.
Est-il réaliste d’espérer un smartphone qui dure une semaine ?
Pas avec la technologie lithium-ion actuelle. Il faudrait une rupture majeure en chimie des matériaux, pas une simple optimisation.
Pourquoi ma batterie perd-elle en autonomie après deux ans ?
Chaque cycle de charge dégrade progressivement les matériaux internes notamment l’anode et le séparateur. C’est un phénomène chimique inévitable.
Les fabricants limitent-ils volontairement l’évolution des batteries ?
Non. Le principal frein n’est pas économique, mais physique et chimique. La sécurité impose des limites strictes.







